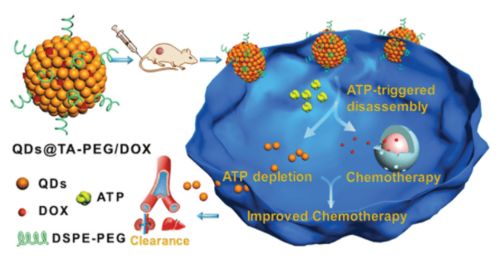
隨著納米技術與生物醫學的深度融合,開發高效、精準的藥物遞送系統已成為現代藥學的前沿課題。其中,將先進納米材料與天然活性成分結合,構建智能響應型遞送平臺,為中藥的現代化和精準化治療帶來了革命性機遇。一種基于三磷酸腺苷(ATP)響應的新型組裝體——量子點(QD)-酚醛納米團簇(NC)系統,展現出將納米藥物靶向遞送至病變部位的巨大潛力,為中藥活性成分的成藥性提升開辟了新路徑。
一、 核心技術:QD-NC組裝體的構建與特性
量子點(QD)作為一種半導體納米晶體,具有優異的光學特性,如尺寸可調的熒光發射、高亮度與光穩定性,使其成為理想的生物成像與示蹤探針。酚醛納米團簇(NC)通常由天然多酚(如單寧酸、沒食子酸等)與金屬離子通過配位作用自組裝而成,具有良好的生物相容性、可降解性及豐富的表面官能團,易于進一步功能化。
通過精密的界面工程與組裝技術,將QD嵌入或共價連接至酚醛NC的網狀結構中,可以形成結構穩定的QD-NC雜化納米組裝體。該組裝體不僅繼承了QD的成像功能,還具備了NC的載藥能力、pH響應性以及通過表面修飾實現主動靶向的潛力。
二、 ATP響應機制:實現病灶部位精準釋放的關鍵
三磷酸腺苷(ATP)是細胞內的“能量貨幣”,其濃度在細胞內外存在巨大差異(細胞內毫摩爾級 vs. 細胞外納摩爾級)。更重要的是,在腫瘤微環境、炎癥部位或缺血/再灌注損傷區域,細胞外ATP濃度會異常升高。這一生物學特性為設計刺激響應型藥物遞送系統提供了完美靶點。
研究者通過對酚醛NC進行功能化修飾,引入ATP適配體或對ATP敏感的化學鍵(如磷酸酯鍵)。當QD-NC組裝體在血液循環中運行時,其結構保持穩定,藥物被有效封存。一旦抵達ATP濃度異常升高的病變組織,高濃度的ATP會作為“鑰匙”,特異性觸發組裝體的結構解離或孔道開放,從而實現藥物的精準、快速釋放。這種“智能開關”機制極大地提高了藥物的利用度,并最大限度地降低了對正常組織的脫靶毒性。
三、 賦能中藥成藥:解決溶解度、靶向性與可視化難題
許多中藥活性成分(如黃酮類、生物堿、萜類化合物)盡管療效確切,但普遍面臨水溶性差、體內代謝快、缺乏靶向性、生物利用度低等成藥性瓶頸。QD-NC-ATP智能遞送系統為這些難題提供了系統性解決方案:
- 增溶與保護:疏水性中藥成分可以被有效負載于QD-NC組裝體的疏水核心或通過π-π堆積、氫鍵等作用吸附于酚醛網絡中,顯著提高其水溶性與穩定性,避免在血液循環中被過早降解或清除。
- 主動與被動靶向協同:一方面,納米尺寸的組裝體可通過增強滲透與滯留(EPR)效應被動富集于腫瘤等病變組織;另一方面,可在組裝體表面進一步偶聯針對病變細胞特定受體的靶向分子(如葉酸、多肽),實現主動靶向。ATP響應機制則確保了藥物在靶點處的可控釋放。
- 治療與成像一體化(診療一體):QD的熒光特性使得整個遞送過程可以被實時、無創地光學成像監控。研究人員可以直觀追蹤納米載體在體內的分布、靶向積累情況以及藥物釋放動力學,實現療效的實時評估與治療方案優化,這正符合現代精準醫療的理念。
四、 前景與挑戰
將ATP響應的QD-NC組裝體應用于中藥納米藥物的靶向遞送,代表了材料科學、分子生物學與傳統藥學交叉創新的重要方向。它不僅能提升經典中藥方劑或單一活性成分的治療效能,還有助于闡明其體內作用機理,推動中藥走向“量化、可視化、精準化”。
該技術走向臨床轉化仍面臨一些挑戰,包括大規模制備的工藝穩定性、組裝體長期毒性與免疫原性的全面評估、體內代謝途徑的詳細解析,以及針對不同中藥成分的個性化載體設計等。未來研究需加強跨學科合作,在確保安全性的前提下,優化系統設計,最終開發出具有國際競爭力的中藥智能納米藥物。
新型ATP響應性量子點-酚醛納米團簇組裝體,巧妙地利用了疾病微環境的生化特征,構建了一個集靶向遞送、智能釋藥與實時成像于一體的多功能平臺。這一前沿技術有望成為破解中藥活性成分成藥性瓶頸的利器,加速中藥現代化進程,為全球患者提供更高效、更安全的治療方案。